喷泉实验(喷泉实验为什么要先挤压滴管 再开止水夹)
能做喷泉实验的条件是什么
能做喷泉实验的条件是:盛气体的烧瓶必须干燥,否则甁中有液体,会使瓶口留下空气,形成的喷泉压力不大。气体要充满烧瓶。实验前应先检查装置的气密性。烧瓶不能漏气。所用气体能大量溶于所用液体或气体与液体快速反应。
条件:气体极易溶于液体。密封性好。形成喷泉的根本原因是压力差。此外,还可以通过温度的改变等情况形成压力差,这样同样可以形成喷泉。 氨气溶于与水。还可是气体与液体反应导致压强变小。
氨气溶解于水,随着滴管中的水进入烧瓶,压强降低,更多氨气溶解,直至水充满烧瓶。实验要求包括:装置必须气密。所选气体应能大量溶解于液体中,或与液体迅速反应。实验要求:为了实现喷泉效果,必须满足以下条件:装置必须保持良好的气密性。
降低气体温度(T):可以通过冷却,如使用冷水浇注或湿毛巾接触瓶底,或者将装置置于低温环境中实现。 增大气体体积(V):可以通过加热(如热水浇注或热毛巾)或改变容器的容积来实现。在化学方法中,气体的溶解度和吸收液的选择对喷泉实验产生直接影响。
喷泉实验的组合有多种,例如NHHCl、SONO2与水组合,酸性气体与NaOH(aq)组合,有机气体与有机溶剂组合,不溶于水的气体通过设计实验条件反应掉也能形成喷泉。喷泉的计算基于充入烧瓶中液体的体积,可以用来计算烧瓶内所盛气体的纯度或平均式量。喷泉实验设计的核心是如何使烧瓶内的气体大量减少。
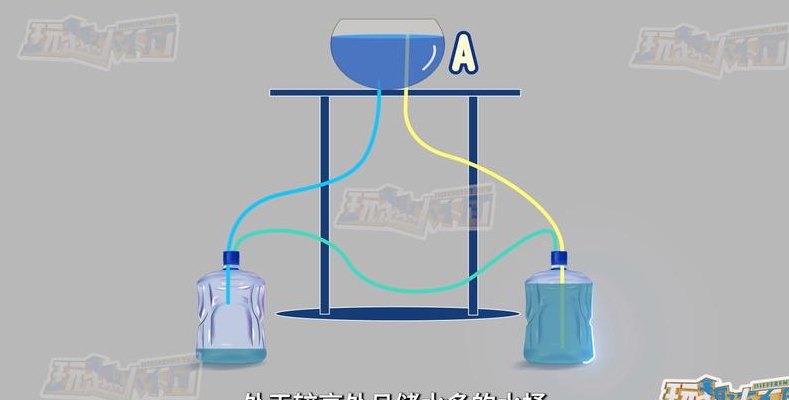
而5也是可以的,反应很快,白色的喷泉(有白色沉淀产生),6,7的反应根据实验观察的话,反应速度比较慢,不能达到快速降低气压的效果(可能和氯气溶解度低也有关系),8的话氨气在汽油中溶解度不大,不满足条件(相似相溶原理),9是可以的,同氨气和水的溶解,形成红色喷泉。
能做喷泉实验的气体有哪些
能做喷泉实验的气体有哪些 氨气和氯化氢气体溶于水的实验可设计成喷泉实验。气态物质发生化学反应生成固态或液态物质的反应可设计成喷泉实验 氯气跟氢氧化钙的反应。在500ml圆底烧瓶里收集满氯气(Cl?),加入约10g氢氧化钙(Ca(OH)2),塞紧带尖嘴的玻璃管的胶塞。
形成喷泉的气体组合多样,例如UTP(常温常压下),NHHCl、SONO2与水的组合能形成喷泉。酸性气体与NaOH(aq)的组合也能形成喷泉,如CO2与NaOH、SO2与NaOH等。有机气体与有机溶剂的组合同样能形成喷泉。此外,ONH2等不溶于水的气体,在设计适当实验条件下与水反应,也能形成喷泉。
NHHCl、HBr、HI等极易溶于水的气体均可做喷泉实验。形成喷泉的组合:(1)utp(常温常压下),nhhcl、sono2与水zhi组合能形成喷泉。(2)酸性气体与naoh(aq)组合能形成喷泉,例如co2与naoh,so2与naoh等。
氨气、氯化氢、二氧化硫、二氧化氮溶于水能形成喷泉实验。这些气体的特点是极易溶于水,溶于水后形成的气压差明显,从而形成喷泉。酸性气体与氢氧化钠溶液也能形成喷泉,如二氧化碳与氢氧化钠,二氧化硫与氢氧化钠等。因为这些气体在碱性溶液中溶解度较大。
喷泉实验原理及图解
1、喷泉实验原理及图解如下:喷泉实验的原理:其实形成喷泉的根本原因是压力差。在教科书上的实验室通过将密闭容器中的气体,溶于某种液体,造成容器内的压强小于外界大气压力(因为体积不变的情况下,气体溶于液体,造成容器内单位体积的气体分子数减少,压强就变小了),从而形成喷泉。
2、喷泉实验的原理:该实验基于压力差异的原理。在实验室设置中,密闭容器内的气体被溶解于液体中,导致容器内压强降低,小于外界大气压强。这种压强差驱动液体通过导管喷出,形成喷泉。此外,通过调节温度等因素来改变压力,同样可以引发喷泉现象。实验中,大气压力将液体压入瓶内,并在尖嘴导管口形成喷泉。
3、喷泉实验的基本原理是:使烧瓶内外在短时间内产生较大的压强差,利用大气压将烧瓶下面烧杯中的液体压入烧瓶内,在尖嘴导管口形成喷泉。喷泉实验是高中阶段最浪漫的实验之一。有位名人说过,喷泉之所以美丽,那是因为它有压力。人生亦复如是。有喷泉,必然伴随着压力。
4、打开玻璃管上的止水夹,用手挤控塑料瓶,使塑料瓶中的氯化氢气体通过玻璃尖嘴进入圆底烧瓶内与氨气接触,即可形成白色的喷烟 。烧瓶内压强减少,浓盐酸会进入烧瓶,产生白色喷泉。
5、抠出小喷泉如下:找一个空的矿泉水瓶;用钉子在矿泉水瓶的瓶盖中心处打上1个小孔;再用钉子把矿泉水瓶围绕一圈打6个或者更多的小孔;打完孔以后把矿泉水瓶装满水,然后迅速盖上瓶盖;演示给小朋友观看“喷泉”小喷泉实验介绍:小喷泉实验是一种物理实验。
6、化学喷泉实验是以下原理 化学喷泉实验是将烧瓶密封住里面的氨气,然后倒置于铁台上,在之前就放好试管与桌子上,盛有酚酞的烧杯相连,这时就会出现一种比较稀奇的现象,原本在底部的酚酞会进入到烧瓶内。其实之所以会出现这样的现象,是因为在倒置的烧瓶当中,密封的氨气是可以溶于水中的。