电子效应(推电子效应和吸电子效应)
电子效应包括哪些
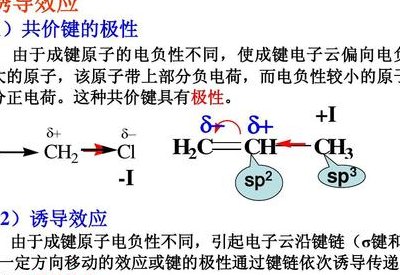
1、电子效应包括诱导效应、共扼效应、场效应和极化效应等, 是在大量实验事实的基础上,总结出来用于解释化学现象的一种理论。[怎么判断共轭效应是吸电子共轭效应还是给电子共轭效应?吸电子基和给电子基是根据什么判断的?]共轭效应只是众多电子效应中的一种。
2、电子效应是在总结大量实验事实的基础上提出的用来解释化学现象的一种理论。电子效应包括诱导效应和共轭效应两种,诱导效应是建立在定域键基础上、短程的电子效应。而共轭效应是建立在离域键的基础上、远程的电子效应,在有机化合物中,往往两种效应同时存在。
3、诱导效应和共轭效应都属于电子效应。区别:(一)存在体系:诱导效应存在σ键中;共轭效应存在于共轭体系中,即单双健交替出现的体系。(二)作用距离:诱导效应是短程的,一般在四键以上(包括四键)此效应可视为零;共轭效应是是远程的,效应存在于整个共轭体系中。
电子对效应作用介绍
光电效应的这一特性表明,光子的能量并非全数转化为光电子的动能,而是有一部分被用于克服原子内部的束缚。这种能量转移是量子力学在微观世界中的一个重要体现,对于理解光与物质的相互作用具有重要意义。
在光电效应中,原子吸收光子的全部能量,其中一部分消耗于光电子脱离原子束缚所需的电离能,另一部分就作为光电子的动能。所以,释放出来的光电子的能量就是入射光子能量和该束缚电子所处的电子壳层的结合能Br之差。
当入射γ光子能量超过02MeV时,产生电子对效应。形成电子对作用就是光子完全被吸收,产生一对粒子,电子和正电子。且随着γ光子能量的增加逐渐成为主要的作用形式。γ光子在核库仑场中完全被吸收,转化成一对正负电子,如图2-9所示。
当原子的内层电子,如4d、4f等,增多时,它们对价电子的排斥力也随之增加,这同样导致平均键能的减小。这一现象在惰性气体元素中尤为明显,如6s2电子对,它们的存在在相对论性效应的框架下被解释,这种效应强调了电子运动速度接近光速时的复杂行为,从而影响了电子对的稳定性和化学键的特性。
电子对效应
1、光电效应的这一特性表明,光子的能量并非全数转化为光电子的动能,而是有一部分被用于克服原子内部的束缚。这种能量转移是量子力学在微观世界中的一个重要体现,对于理解光与物质的相互作用具有重要意义。
2、当入射光子能量大于2m0c2(即02MeV)时,入射γ光子在核库仑场作用下能量完全被吸收,电子从负能级跃迁到正能级,同时放出正、负电子,称电子对效应。如图2-2-6所示,其运动方向在光子前进方向。
3、当原子的内层电子,如4d、4f等,增多时,它们对价电子的排斥力也随之增加,这同样导致平均键能的减小。这一现象在惰性气体元素中尤为明显,如6s2电子对,它们的存在在相对论性效应的框架下被解释,这种效应强调了电子运动速度接近光速时的复杂行为,从而影响了电子对的稳定性和化学键的特性。
4、当入射光子能量大于2 m0c2(即02MeV)时,入射γ光子在核库仑场作用下能量完全被吸收,电子从负能级跃迁到正能级,同时放出正、负电子,称电子对效应。如图2-2-6所示,其运动方向在光子前进方向。
5、形成电子对效应包括正负电子对的生成和湮没两个过程。由式(2-11)可知,只有当入射光子能量hν>02MeV时,才可能有电子对的形成。形成电子对的几率与作用物质原子序数平方成正比,还与γ光子能量成正比。
6、电子对效应的截面бP与吸收物质原子序数Z和入射光子能量有关。在入射光子能量大于02MeV的任何范围内,бP与Z2 成正比。
有机化学中的电子效应有哪两种
1、电子效应是在总结大量实验事实的基础上提出的用来解释化学现象的一种理论。电子效应包括诱导效应和共轭效应两种,诱导效应是建立在定域键基础上、短程的电子效应;而共轭效应是建立在离域键的基础上、远程的电子效应,在有机化合物中,往往两种效应同时存在。
2、在有机化学的世界里,分子间的电子行为由两种主要效应主导:诱导效应(I)和共轭效应(C)。诱导效应,通常被称为定域效应,起源于分子中短程的、四键或更多键的结合。这种效应在较小的范围中发挥作用,对于四键或以上的结构,其影响可以忽略不计,视为零。
3、电子效应 1共轭效应:单双键交替出现的体系称为共轭体系。在共轭体系中,由于原子间的相互影响而使体系内的π电子(或P电子)分布发生变化的一种电子效应称为共轭效应。凡共轭体系上的取代基能降低体系的π电子密度,则这些基团有吸电子的共轭效应,用-C表示。
4、电子效应包括诱导效应、共轭效应、场效应和极化效应等,是在大量实验事实的基础上,总结出来用于解释化学现象的一种理论。诱导效应是基于定域键基础上的短程电子效应;共轭效应是基于离域键基础上的远程的电子效应。在有机化合物中,往往同时存在以上两种电子效应。也就是说,最主要的两个电子效应,就是诱导效应和共轭效应。
什么叫电子效应,空间效应?有机没学好
1、电子效应:在大多数反应中,由于取代基(与氢原子相比)倾向于给电子或是吸电子,使分子某些部分的电子密度下降或上升,使反应分子在某个阶段带有正电荷(或部分正电荷)或负电荷(或部分负电荷)的效应。电子效应可以通过多种方式传递,如诱导效应、共轭效应、场效应等。
2、电子效应:由于取代基倾向于给电子或是吸电子,使分子某些部分的电子密度下降或上升,使反应分子在某个阶段带有正电荷(或部分正电荷)或负电荷(或部分负电荷)的效应。诱导效应和共轭效应都属于电子效应。区别:(一)存在体系:诱导效应存在σ键中;共轭效应存在于共轭体系中,即单双健交替出现的体系。
3、电子效应可以影响物质的性质,这个总结是很好的。官能团影响性质,哪怕是一个刚接触有机化学的人都了解,这是个大方向。可具体到纷繁复杂的有机化合物 电子效应包括诱导效应、共轭效应、场效应和极化效应等,是在大量实验事实的基础上,总结出来用于解释化学现象的一种理论。
4、电子效应可以通过多种方式传递,如诱导效应、共轭效应、场效应等。目前,电子效应已普遍用于解释分子的性质及其反应性能。分类 场效应 取代基在空间可以产生一个电场,对另一头的反应中心有影响,这种空间的静电作用称为场效应。共轭效应 单双键交替出现的体系称为共轭体系。
5、个人认为:电子效应是根据原子或基团之间的电负性大小来判断,电负性大的对电负性小基团产生的效应就是吸电子,反过来就是推电子。共轭是有双键,三键,苯环等电子在气结构上可以流动,有π-π共轭, p-π共轭,σ-π超共轭,推和吸主要是跟电负性来判断的。
6、虽然我还没学有机……不过依稀记得一点……第一道题。
大学有机化学.诱导效应,电子效应,共轭效应区别是什么。。?
1、区别:(一)存在体系:诱导效应存在σ键中;共轭效应存在于共轭体系中,即单双健交替出现的体系。(二)作用距离:诱导效应是短程的,一般在四键以上(包括四键)此效应可视为零;共轭效应是是远程的,效应存在于整个共轭体系中。(三)极性变化:诱导效应极化变化是单一方向;共轭效应极性交替出现。
2、电子效应对有机化合物化学性质的影响主要体现在诱导效应、共轭效应、场效应。诱导效应:当一个电负性较大的原子(如卤素)与一个碳原子成键时,会产生诱导效应。这种效应会使得与碳原子相连的其他原子的电子云偏向于电负性较大的原子,导致碳原子的电子云密度下降,使得该碳原子更容易被亲核试剂进攻。
3、诱导效应是基于定域键基础上的短程电子效应;共轭效应是基于离域键基础上的远程的电子效应。在有机化合物中,往往同时存在以上两种电子效应。也就是说,最主要的两个电子效应,就是诱导效应和共轭效应。文章的主要内容就是解释这两个电子效应。当然,我只是浅显地说明,整理一下,加上我自己看来的东西和自己的部分理解。
4、电子效应,如同投资与合作 诱导效应,如同一笔借款投资,它由原子间的电负性差异驱动,电子云沿着化学键流动,沿着原子链产生影响。然而,这种影响并非一蹴而就,而是逐渐递减,如同借钱的本金和利息随距离而减少。衡量诱导效应的尺度是烷基氢,+I表示吸引电子,-I则表示推斥电子。
5、相比之下,共轭效应则是基于离域键的,具有远程性质。它并非局限于局部区域,而是影响整个共轭体系,即分子中那些共享电子的连续键链。这种效应是分子结构中一个显著的长程影响因素,对于分子的电子性质和化学行为至关重要。
6、个人认为:电子效应是根据原子或基团之间的电负性大小来判断,电负性大的对电负性小基团产生的效应就是吸电子,反过来就是推电子。共轭是有双键,三键,苯环等电子在气结构上可以流动,有π-π共轭, p-π共轭,σ-π超共轭,推和吸主要是跟电负性来判断的。