氢键是什么(氢键是什么作用力)
氢键是什么?
1、氢键是一种分子间相互作用。氢键存在于分子之间,是由氢原子与电负性较强的原子之间的相互作用形成的。这种相互作用是由于氢原子与电负性较强的原子之间的电子云重叠产生的吸引力所致。氢键的强度介于化学键和范德华力之间,比一般的分子间作用力稍强一些。
2、氢键是一种分子间的相互作用力。氢键的形成是由于某些分子中的氢原子与另一个分子中的强电负性原子之间的相互作用。这种相互作用主要是由于氢原子与电负性原子之间的电子云重叠,导致电子云之间的吸引作用增强。这种吸引力不同于普通的化学键,因为它存在于分子之间,而不是单个分子的内部。
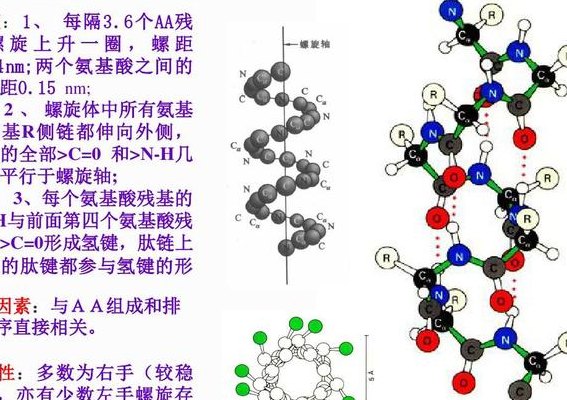
3、氢键的结合能是2—8千卡(Kcal)。因多数氢键的共同作用,所以非常稳定。在a-螺旋的情况下是N-H…O型的氢键,DNA的双螺旋情况下是N-H…O,N-H…N型的氢键,因为这样氢键很多,因此这些结构是稳定的,此外,水和其他溶媒是异质的,也由于在水分子间生成O-H…O型氢键。
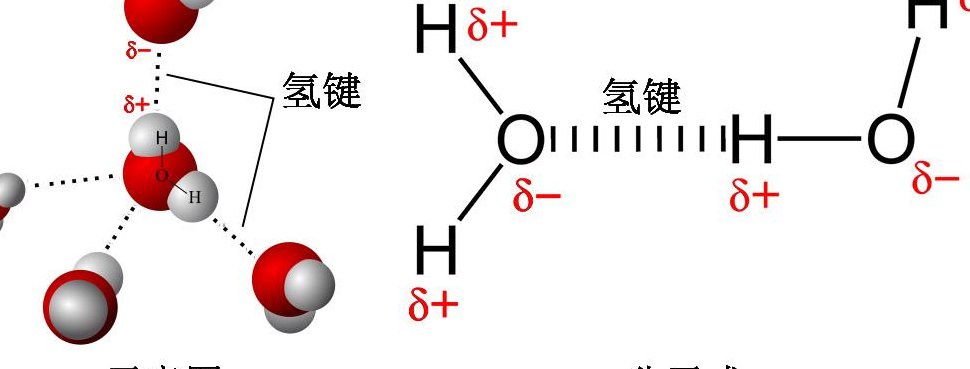
4、氢原子与电负大、半径小的原子X(氟、氧、氮等)以共价键结合,若与电负大的原子Y(与X相同的也可以)接近,在X与Y之间以氢为媒介,生成X-H···Y形式的一种特殊的分子间或分子内相互作用,称为氢键。
5、氢键是一种特殊的分子间作用力,通常发生在氢原子与氧、氮、氟等电负性较强的原子之间。由于这些原子的电子分布特点,它们对氢原子产生一定的吸引力,这种力就是氢键。氢键的形成需要满足一定的条件:一是要有氢原子,二是与氢原子相连的基团要有电负性较强的原子。
什么是氢键,它的定义是什么?
1、氢键的定义 氢原子与电负性大的原子X以共价键结合,若与电负性大、半径小的原子Y(O F N等)接近,在X与Y之间以氢为媒介,生成X-H…Y形式的一种特殊的分子间或分子内相互作用,称为氢键。
2、氢键的定义:氢原子与电负大的原子X以共价键结合,若与电负大、半径小的原子Y(O F N等)接近,在X与Y之间以氢为媒介,生成X-H…Y形式的一种特殊的分子间或分子内相互作用,称为氢键。典型的氢键中,X和Y是电负很强的F、N和O原子。
3、分子内氢键降低沸点但提高稳定性。氢键既可以是分子间氢键,也可以是分子内的。其键能最大约为200kJ/mol,一般为5-30kJ/mol,比一般的共价键、离子键和金属键键能要小,但强于静电引力。氢键对于生物高分子具有尤其重要的意义,它是蛋白质和核酸的三和四级结构得以稳定的部分原因。
4、氢键的定义 氢键是一种特殊的分子间相互作用,发生在氢原子与电负性较高的原子之间,如氧、氮、氟等。这种相互作用是由于氢原子与电负性原子之间的电子云相互作用形成的吸引力。在氢键中,氢原子作为一个连接桥梁,通过其电子云与另一个分子的电负性原子形成强烈的吸引力。
5、氢键是一种分子间或分子内非共价键,由氢原子和电负性较强的原子X(如F、O、N等)之间形成。氢键的形成是由于电负性较强的X原子对H原子产生的强烈吸引作用,使得H原子偏向于X原子,从而使得X-H键的极性增强。
6、氢键结合的情况如果写成通式,可用X-H…Y表示。式中X和Y代表F,O,N等电负性大而原子半径较小的非金属原子。X和Y可以是两种相同的元素,也可以是两种不同的元素。(4)对氢键的理解。氢键存在虽然很普遍,对它的研究也在逐步深入,但是人们对氢键的定义至今仍有两种不同的理解。
什么是氢键
1、氢键是一种分子间的相互作用力。氢键的形成是由于某些分子中的氢原子与另一个分子中的强电负性原子之间的相互作用。这种相互作用主要是由于氢原子与电负性原子之间的电子云重叠,导致电子云之间的吸引作用增强。这种吸引力不同于普通的化学键,因为它存在于分子之间,而不是单个分子的内部。
2、与负电性大的原子X(氟、氯、氧、氮等)共价结合的氢,如与负电性大的原子Y(与X相同的也可以)接近,在X与Y之间以氢为媒介,生成X-H…Y形的键,这种键称为氢键。氢键的结合能是2—8千卡(Kcal)。因多数氢键的共同作用,所以非常稳定。
3、氢键是一种分子间的相互作用力。氢键是由氢原子与强电负性元素之间的共价键相互作用而形成的。在分子间,由于氢原子的存在,使得与强电负性元素相连的氢原子具有一定的正电性,可以与附近分子中的强电负性元素形成吸引力,从而产生氢键。
4、氢原子与电负大、半径小的原子X(氟、氧、氮等)以共价键结合,若与电负大的原子Y(与X相同的也可以)接近,在X与Y之间以氢为媒介,生成X-H···Y形式的一种特殊的分子间或分子内相互作用,称为氢键。
氢键是什么
1、与负电性大的原子X(氟、氯、氧、氮等)共价结合的氢,如与负电性大的原子Y(与X相同的也可以)接近,在X与Y之间以氢为媒介,生成X-H…Y形的键,这种键称为氢键。氢键的结合能是2—8千卡(Kcal)。因多数氢键的共同作用,所以非常稳定。
2、氢键是一种分子间的相互作用力。氢键的形成是由于某些分子中的氢原子与另一个分子中的强电负性原子之间的相互作用。这种相互作用主要是由于氢原子与电负性原子之间的电子云重叠,导致电子云之间的吸引作用增强。这种吸引力不同于普通的化学键,因为它存在于分子之间,而不是单个分子的内部。
3、氢键是一种分子间相互作用。氢键存在于分子之间,是由氢原子与电负性较强的原子之间的相互作用形成的。这种相互作用是由于氢原子与电负性较强的原子之间的电子云重叠产生的吸引力所致。氢键的强度介于化学键和范德华力之间,比一般的分子间作用力稍强一些。